Какие части тела ученые научились пересаживать, а какие - нет
Ева Онтиверос
Би-би-си
27 апреля 2018
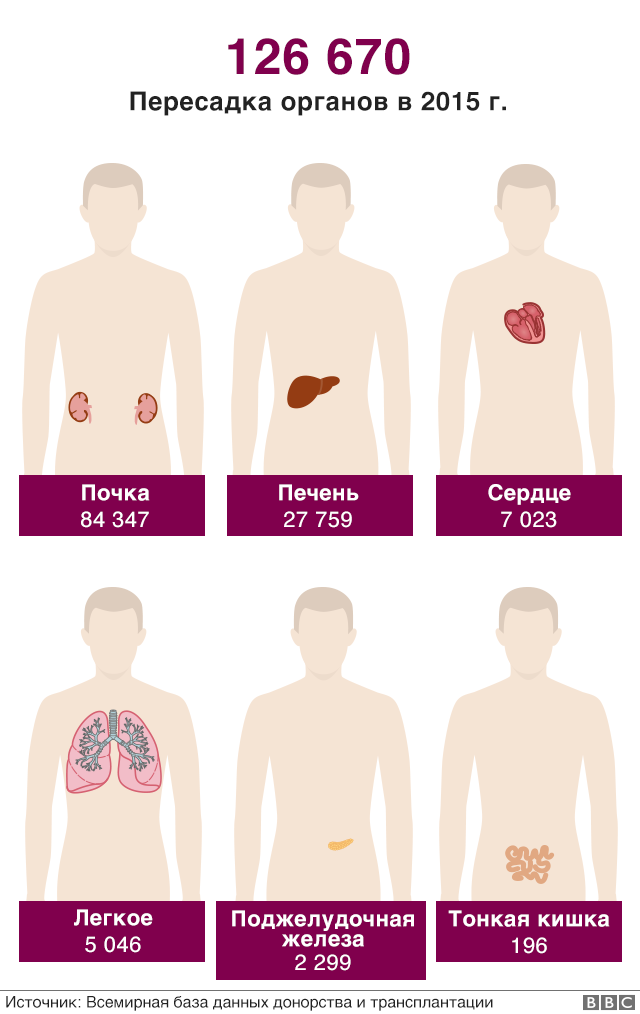
В 2015 году в мире было произведено в общей сложности более 126 тысяч операций по пересадке органов. Это в среднем 14,5 трансплантаций в час.
В подавляющем большинстве случаев речь шла о пересадке частей тела, необходимых для продолжения жизни. Большая часть (41,8%) пришлась на трансплантацию почек, следом идут печень и сердце.
В последние годы растет также число пересадок легких, поджелудочной железы и тонкой кишки.
Врачи научились пересаживать не только органы, но и различные ткани. Достаточно распространены трансплантации костного мозга, сухожилий, роговой оболочки глаза, кожи, сердечных клапанов, нервов и вен.
Однако многие части тела заменить по-прежнему не получается. Какие и почему?
ГоловаТрансплантация головы невозможна - и едва ли будет возможна в обозримом будущем.
"Мы должны сосредоточиться на достижимых вещах. За последние 50 лет мы многого добились в пересадке любых частей тела ниже шеи", - говорит Габриэль Ониску, консультант-трансплантолог в Королевской больнице Эдинбурга и секретарь Европейского общества по трансплантации органов.
С ним соглашается Лорна Мейсон, хирург-трансплантолог и президент Британского трансплантологического общества. Ведь цель врачей - сохранить жизнь как можно большему числу людей, поэтому необходимо "выбирать наиболее реалистичные опции".
Помимо очевидного философского спора (пересаживают ли мозг в тело или мозгу пересаживают тело?), главной трудностью такого рода операции стала проблема соединения головного мозга со спинным.
Большинство операций по трансплантации сталкиваются с проблемой успешного соединения кровеносных сосудов, однако спинной мозг, который отвечает за движение, - это сеть весьма специализированных нервных клеток, называемых нейронами.
Клетки такого типа передают информацию с помощью электрических и химических сигналов, и если их повредить, то заменить их или снова связать воедино будет невозможно.
Это объясняет, почему на сегодняшний день серьезные травмы спинного мозга часто остаются неизлечимыми.
Доктор Мейсон говорит, что в случае травмы или повреждения головного мозга из-за болезни "существуют более реалистичные опции - вроде замены клеток там, где это возможно сделать".
Ученые разрабатывают клеточную терапию, которая в некоторых случаях позволит нейронам регенерироваться и развиваться.
"Клеточная терапия может остановить, а в некоторых случаях даже повернуть вспять развитие дегенеративного заболевания тканей головного мозга, - говорит доктор Мейсон. - Лечение такого рода может помочь пациентам с деменцией или рассеянным склерозом".
Сетчатка глазаСетчатка находится в задней части глазного яблока и отвечает за преобразование света в видимую картинку
Хотя успешные операции по пересадке роговицы проводятся уже несколько десятилетий, по-прежнему невозможно пересадить сетчатку - внутреннюю часть глазного яблока, которая позволяет нам видеть предметы и изображения.
Эта часть тела опять же включает в себя множество разветвленных нервных связей, так что трансплантация столь сложной нейронной структуры пока остается за пределами современных технических возможностей.
И хотя этими двумя органами список совершенно невозможных трансплантаций ограничивается, существуют операции по пересадке, которые пока еще не стали для хирургов привычным делом.
Желчный пузырьПосле любой операции по пересадке пациенту придется провести остаток жизни на иммуноподавляющих препаратах, которые позволят избежать отторжения нового органа, и в случае желчного пузыря это просто того не стоит.
"Любая трансплантация - это баланс между благом пациента и неизбежными последствиями: восстановлением после такой операции и необходимостью принимать лекарства на протяжении всей оставшейся жизни", - объясняет Лорна Мейсон.
Желчный пузырь находится под печенью и содержит желчь - жидкость, которая выделяется в тонкую кишку и помогает пищеварению. Он упрощает вашу жизнь, но не является жизненно необходимым.
"Это как аппендикс. Если в желчном пузыре регулярно образуются камни или он поражен болезнью, полезнее для здоровья будет его удалить. Мы можем прекрасно жить и без него", - говорит доктор Ониску.
В таком случае пациенту рекомендуется изменить режим питания и образ жизни, чтобы упростить пищеварение.
СелезенкаДоктор Ониску говорит, что селезенка - это немного другой случай, так как это "орган, который фильтрует, ремонтирует и сохраняет красные кровяные клетки". Но при этом, по его словам, селезенка также не является необходимой для поддержания жизни, так что к ней применим тот же принцип.
После удаления селезенки пациент должен всю жизнь принимать антибиотики - но, опять же, все дело в балансе и в том, что более эффективно для пациента.
"Удаление и антибиотики - это меньший риск, чем перенести операцию по пересадке и до конца жизни принимать медикаменты, чтобы избежать отторжения", - уверяет Мейсон.
Будущее трансплантацииОсновное внимание всегда будет уделяться тем частям тела, которые поддерживают жизнь, однако, говорит доктор Ониску, "органы пересаживают по какой-то причине, это должно удовлетворять нужду пациента".
"Вот почему мы, к примеру, делаем пересадку матки, - объясняет он. - Жить без этого органа можно, но пациентка может почувствовать, что не выполнит предназначение своей жизни, если у неё не будет детей. А пересадка матки удовлетворит нужду этой конкретной пациентки".
Врачи уверены, что в будущем пациентам можно будет помогать не только при помощи традиционных операций по пересадке органов - вроде печени, сердца или легкого, - но и за счет регенерации и трансплантации клеток.
"Идеальный пример - пересадка клеток островков Лангерганса для лечения диабета, - говорит доктор Ониску, имея в виду крохотные скопления клеток, которые выделяют инсулин. - Для решения проблемы мы пересаживаем клетки из поджелудочной железы, а не всю железу целиком".
По мере того как растет спрос, медики изучают более сложные стратегии лечения, выходящие за пределы пересадки органов и клеточной терапии - и трансплантация все чаще дополняется регенеративной медициной, новыми технологиями и биоинженерией.
Ониску говорит: "Мы изучаем искусственные органы, то есть органы, которые восстанавливаются при помощи стволовых клеток, и, вероятно, даже органы, выращенные в иной среде, - ксенотранспланты". Так называются донорские органы или ткани, имеющие животное происхождение, а также человеческие органы, выращенный в теле животного для последующей пересадки людям.
Мейсон обращает внимание, что в конечном итоге "успех пересадки сводится к результатам командной работы и вклада огромной команды экспертов".
https://www.bbc.com/russian/features-43907307===============================
Ученые вырастили искусственную сетчатку в пробиркеНиколай Воронин
Корреспондент по вопросам науки и технологий
13 октября 2018
В лаборатории Университета Джонса Хопкинса искусственно выращивают человеческие глаза - точнее, внутреннюю оболочку глаза, сетчатку.
Пока что ее нельзя использовать для пересадки, и ученые надеются решить другую проблему: понять, каким образом мы различаем цвета, и помочь людям, которые испытывают с этим проблемы.
Сетчатка прилегает к зрительному нерву, и именно там формируется изображение, поступающее в мозг.
Миллионы футбольных болельщиков - дальтоники. Как они видят ЧМ-2018?
Давно известно, что в нашем глазу есть три вида цветовых рецепторов (так называемых колбочек), воспринимающих красный, зеленый или голубой цвет. Однако как именно происходит их формирование, до сих пор понятно не до конца. У большинства млекопитающих есть только два вида рецепторов.
В процессе выращивания искусственной сетчатки из стволовых клеток ученые обнаружили, что первыми формируются "синие" колбочки - а уже за ними "зеленые" и "красные". Более того, удалось найти способ активировать - или, наоборот, блокировать - рост этих фоторецепторов при помощи гормонов. А это открывает возможность лечения дальтонизма и возрастных изменений сетчатки.
На сегодняшний день дальтонизм неизлечим, а частичную потерю зрения вследствие дегенерации сетчатки пытаются лечить инъекциями в глаз стволовых клеток, однако эта терапия далеко не всегда дает желаемый эффект.
https://www.bbc.com/russian/features-45817790================================
Женщина родила здорового ребенка после пересадки матки от мертвого донора 5 декабря 2018
Бразильские врачи сообщили о прорыве в репродуктивной медицине: женщина выносила и родила ребенка после того, как ей была пересажена матка от умершего донора. В результате родилась здоровая девочка.
10-часовая операция по трансплантации органа и последующая репродуктивная терапия проходила в бразильском Сан-Паулу в 2016 году, но известно о ней стало только сейчас после публикации в медицинском журнале Lancet.
В истории медицины были 39 случаев успешной пересадки матки от живых доноров, в том числе от матерей, согласившихся отдать матку своим дочерям. В результате этих операций родились 11 детей.
32-летняя реципиентка родилась с пороком развития матки. Донором матки стала мать троих детей, женщина старше 40, умершая от кровоизлияния в мозг. До этого она завещала свое тело науке.
У пациентки, которой пересадили матку - синдром Майер-Рокитанского-Кюстер-Хаузера (МРКХ) - болезнь, встречающаяся у одной женщины из 4500 и заключающаяся в недоразвитии матки, яичников и наружных половых органов.
Однако яичники пациентки оказались нормально развиты, и врачи сумели извлечь яйцеклетки, оплодотворить их и заморозить.
Женщина получала специальные препараты для ослабления иммунитета, призванные предотвратить отторжение пересаженного органа.
Спустя примерно шесть недель после операции у женщины восстановился менструальный цикл. Через семь месяцев ей была проведена процедура ЭКО.
В результате нормальной здоровой беременности 15 декабря 2017 года посредством кесарева сечения родилась здоровая девочка весом 2,5 кг.
"Первые операции по пересадке матки от живых доноров были прорывом в медицине, они открыли возможность деторождения для многих бесплодных женщин", - сказал доктор Дани Айзенберг из госпиталя Сан-Паулу.
"Однако потребность в живом доноре была своего рода ограничением, такие доноры редки, чаще всего это близкие родственники или преданные друзья".
По словам доктора Срджагна Сасо из Имперского колледжа Лондона, достигнутые результаты впечатляют. "Они позволяют расширить возможности донорства, снизить цены и избежать хирургических рисков для доноров".
https://www.bbc.com/russian/news-46452890